技术支持Technical Support
联系我们CONTACT US
 400-999-210024小时服务热线
400-999-210024小时服务热线
文献解读 | 智能纳米抗肿瘤药物带来新发现
来源:Pricella 浏览量: 发布时间:2021-12-15 10:48:19
通常我们所说的化疗,即通过化学药物消灭癌细胞,是最常用的治疗癌症的方法之一。化疗的治癌功效虽然明显,但是也会带来骨髓抑制、恶心呕吐、脱发等非常严重的副作用。
这是因为化学药物常常“敌我不分“,把正常细胞当成癌细胞去攻击。因此,寻求能够精准作用于癌细胞的靶向药物迫在眉睫。
纳米颗粒作为抗肿瘤药物,有着天生的优越性,主要体现在两个方面:第一,纳米颗粒具有高渗透长滞留效应(EPR),比起正常组织,更容易渗透进肿瘤组织,并且滞留时间长;第二,纳米颗粒可以灵活变换尺寸和容积,更好地发挥抗肿瘤效果。
尽管已经拥有了相对的优势,但纳米药物的研发仍然面临许多困难。比如,纳米颗粒释放药物产生的效应物质容易被降解,同时,药物还可能被缺氧细胞地P-糖蛋白泵出来,导致药物的利用率下降。所以,如何加强纳米颗粒释放药物的渗透和滞留是急需突破的事情。
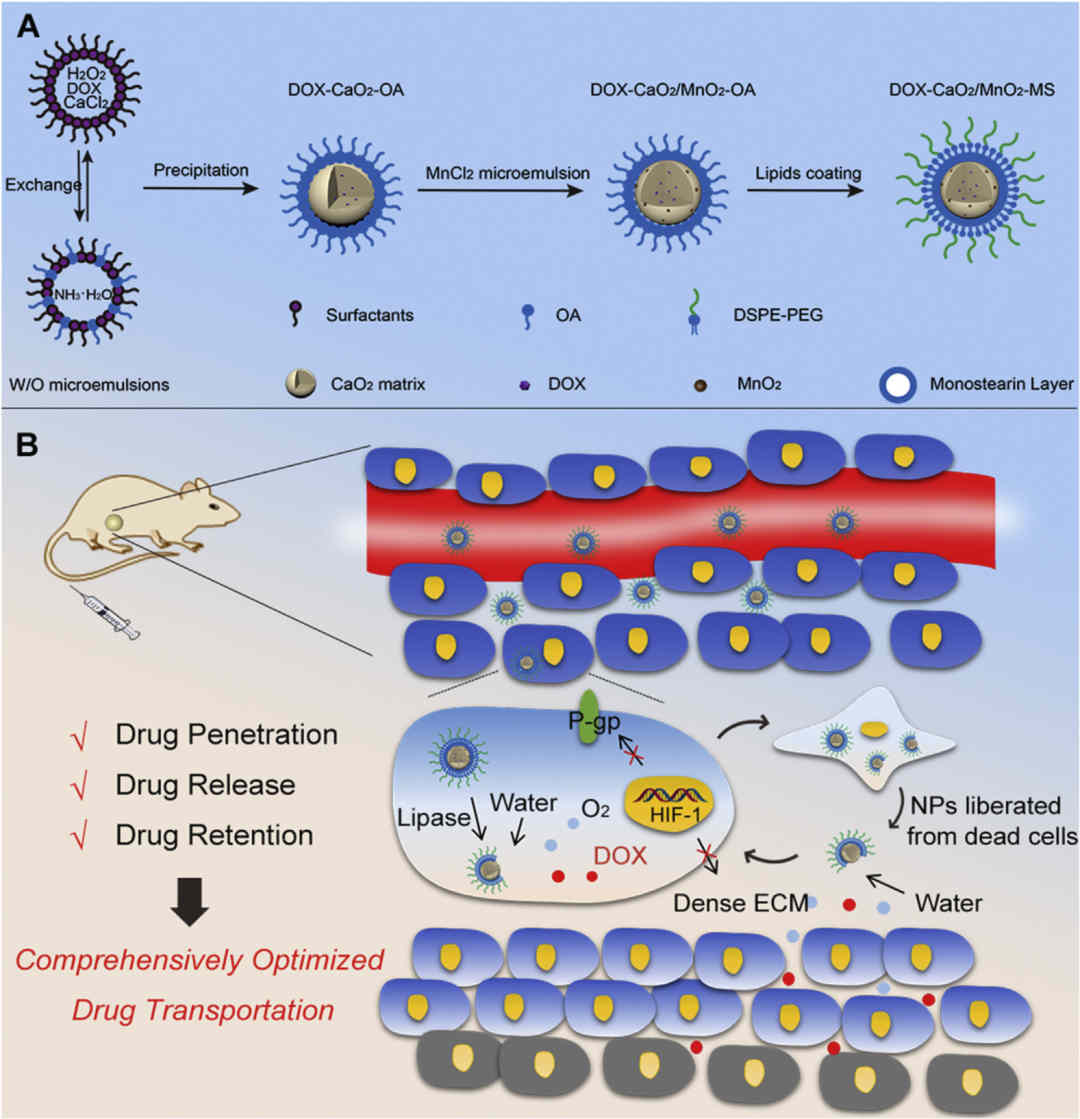
▲ DOX- CaO2/MnO2 -MS纳米药物的作用原理
华中科技大学的Jun Luo, Xiang Ma,和Guangya Xiang团队,合作研发了一种用monostearin(MS)包被CaO2/MnO2的新型纳米载体,用它装载阿霉素(DOX)并作用于肿瘤时,MS外壳被肿瘤细胞中的脂肪酶水解,经过一系列化学反应,DOX和氧气从载体中释放,成功消灭肿瘤细胞。
死亡的肿瘤细胞继续释放已经暴露核心的载体,DOX在肿瘤细胞外基质中释放和扩散,进入肿瘤组织深处。同时,氧气减少了胞外基质中的胶原沉积,并抑制P-糖蛋白,有效增加药物在肿瘤组织中的滞留时间。
这项研究于2021年1月19日发表在国际期刊Acta Pharmaceutica Sinica B(IF=11.413(2021)),题为《A smart O2-generating nanocarrier optimizes drug transportation comprehensively for chemotherapy improving》。Xiaojuan Zhang、Chuanchuan He、Guangya Xiang为该研究的设计者。


▲ 该研究发表于国际期刊Acta Pharmaceutica Sinica B
那么,这种新型纳米药物抗肿瘤效果究竟如何呢?
首先,研究团队通过在人卵巢癌细胞系SKOV3上做体外测试,发现药物很快被细胞吸收。他们在培养基里添加DOX- CaO2/MnO2 -MS纳米药物,0.5小时后在细胞质中检测到DOX,4小时后DOX进入细胞核。
对SKOV3进行缺氧培养,发现缺氧条件下药物对细胞的毒性增强。用该纳米药物处理SKOV3的MCTS(multicellular tumor spheroids)模型,24小时后即可到达组织深处,继续观察后,发现它能够很好地抑制MCTS模型的生长。
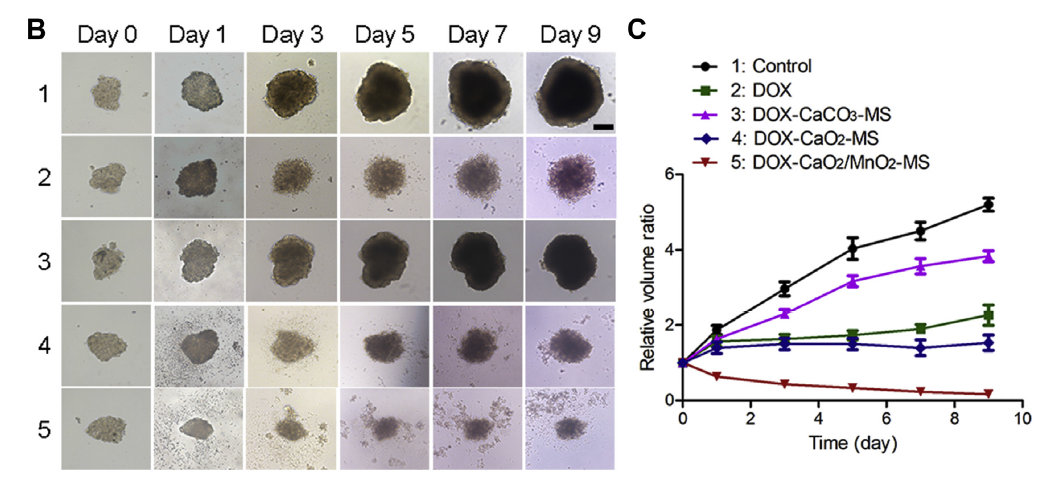
▲ DOX- CaO2/MnO2 -MS纳米药物对SKOV3细胞MCTS模型的生长抑制作用
其次,向SKOV3细胞异种移植的裸鼠注射DOX- CaO2/MnO2 -MS纳米药物(DiR标记),而注射后仅仅4小时,就在肿瘤组织中观察到荧光,说明该药物非常迅速且精准地靶标到肿瘤。相比于游离DOX,DOX- CaO2/MnO2 -MS,它对肿瘤的抑制效果更加明显。更令人欣喜的是,被注射新药的小鼠,其体重没有明显下降,这证明了药物具有安全性。
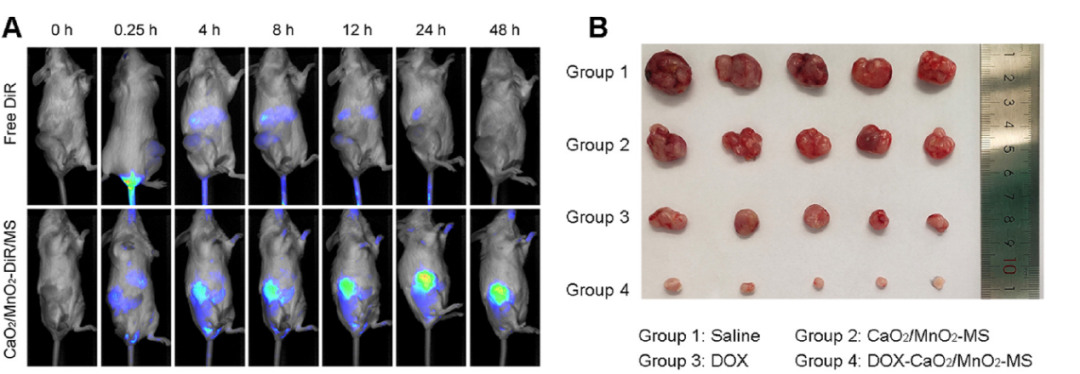
▲ 向模型鼠注射DOX- CaO2/MnO2 -MS后药物的定位及肿瘤的大小对比
DOX- CaO2/MnO2 -MS纳米药物,因其巧妙地设计,不仅能够将核心药物准确地递送到肿瘤组织,还能通过氧气抑制药物泄露,增加药物在肿瘤中滞留的时间,协同加强抗肿瘤疗效。该研究成果,在其他依赖于氧气的癌症治疗方法中,如光动力治疗,放射治疗和免疫治疗,将有望发挥巨大的应用潜力。
本研究使用的普诺赛产品
产品名称 | 产品货号 |
CL-0215 |
原文链接:https://doi.org/10.1016/j.apsb.2021.04.021
温馨提醒:
如果您想要了解或选购细胞系或者原代细胞,请点击我要选购,有任何疑问也可以点击右方的在线咨询,专业技术人员将为您提供解答。



































